
�P�D�S�[�ד��̗Տ��I�Ӌ`
�@�@�S�[�ד��ł́A�S�[�S�̂Ƃ��Ă̂܂Ƃ܂����������Ȃ��A�S�[�͖������ɂR�T�O�`600/���̕s�K���ȋ������N�����B��ʂɐS���o�ʂ͐�s���k�̊g�����̒����ɔ�Ⴗ��@(Starling�̐S���@���j�B�@�S�[�ד��ł͖[���`���n�i�[�����߁A�q�X���j�̓`���\�̋����͈͓��ɂ����đ����̋�����S���ɓ`���邪�A���̍ہA�S�������Ԋu���Z���Ɗg�������Z���Ȃ�A�����ւ̏\���Ȍ��t�������N����Ȃ����߁A�S���o�ʂ��ቺ���A���������Ŗ������ӂ꓾����x�̍������k���N���������o���Ȃ��B���̂��߁A�S�����Ɩ������Ƃ͈�v�����A��҂��O�҂ɔ�ׂď��Ȃ��Ȃ�B����𖬔�����(pulse
deficit)�ƌĂсA���ꂪ������(��10/���j�|���v�Ƃ��Ă̐S���̋@�B�I����������Q���A�S�s�S�Ɋׂ�B�@���̂悤�Ȗ����������Ղ����Ƃ��S�[�ד��̌��s���ԓI�����̂P�ł���B��ʂɁA������������10/���ȏ�ɂȂ�ƐS���̌������ቺ���A���҂͘J�쎞�ɐS�����i��ċz������Ղ��Ȃ邽�߁A�W�M�^���X���b���h�R��Ȃǂ�p���Ė��������̏�����}�邱�Ƃ��K�v�ƂȂ�B
�@���̑��̐S�[�ד��̗Տ��I�Ӌ`�Ƃ��ẮA�S�[�������`���ɂ�铮���ǐ��i���Ƃɔ]�ǐ��j�̔���������B�S�[���Ɍ`������錌���͑傫���A���ꂪ�����ɂ���Ĕ]������ǂ��Đ�����]�[�ǂ͔]�������̓����d�����a�ςɋN������]�[�ǂɔ�ׂĒ������傫���A�a����d���ꍇ�����������\����d�Ăł���B���̂��߁A�����S�[�ד���ł͍R�Ì���i���[�t�@�����j�����ɂ�錌���`���\�h���s��˂Ȃ�Ȃ��B
�@���}�͐S�[�ד����m�X�ً���ǂ̍��[���Ɍ`�����ꂽ���V�{�[�����̒f�w�S�G�R�[�}�ł���B
| �S�[�ד���̍��[���ɔF�߂�ꂽ���V������ |
2. �S�[�ד��̐S�d�}����
�@�S�[�ד��̓����I�S�d�}�����Ƃ��ẮA
�@�@�i�P�j�@�o�g�̏����A
�@�@�i�Q�j�@���g�̏o���A
�@�@�i�R�j�@��ΐ��s����
�@�̂R�������グ����B�S�[�ד��̍ۂɂ́A�h���͖[�����ߓ��Ɏ�X�̒��x�ɐ��ʂ��ĒE���ɂ��N�����i���s�`���C�@concealed
conduction�j�A�s�K���ȕs���������B���̂��ߐS�[�����̐S���ւ̓`���͕s�K���ƂȂ�A�S���K�������Ȃ��s�����������i��ΐ��s����,
arrhythmia absoluta�j�B
�R�D�S�[�ד��̌����A��b����
�@�S�[�ד��̊�b�����Ƃ��ẮA����A�������A���A�a�A�������S���a�A�S���ٖ��ǁi���Ƃɑm�X�ً���j�A�������S���A�b��B�@�\���i�ǂȂǂ�����B�X�̎����ʂɌ��ĐS�[�ד��̍������������̂͑m�X�ٖ��ǁA�b��B�@�\���i�ǂł��邪�A���ۂɑ�������S�[�ד��ɂ��Č����������A�������S���a�Ȃǂ��ł������B
�@����́A�S�[�ד��͉���Ƌ��ɏo�������������������A�������A�������S���a�͍��N�҂ɑ������ƂɋN�����Ă���B�������A�S�[�ד��̒��ɂ͑S����b�������Ȃ��Ⴊ��������A�ulone
atrial fibrillation�v�ilone���ǓƂȁj�ƌĂ�A�]���́u�������ہv�ɂ��Ƃ����Ă����B����͖��Q�ȕs�����ƍl�����Ă������A�ߔN�A���̂悤�Ȋ�b�������Ȃ��S�[�ד����S�[�������`������]�ǐ����N�����ꍇ�����Ȃ��Ȃ����Ƃ��F������A���̗\�h�̂��߂̍R�Ì���Ö@�̕K�v�����F�������悤�ɂȂ����B
�@�S�[�ד��̓d�C�����w�I�����Ƃ��ẮA
�@�@�i�P�j�@���Lj��q�A
�@�@�i�Q�j�@�ێ��@�\
�@�̂Q�̗v�f�ɕ����čl���邱�Ƃ��K�v�ł���B
�@���Lj��q�Ƃ��Ăُ͈����h���`�����l�����Ă���A�Տ��I�ɂ��S�[�̓d�C�h���ŐS�[�ד���U���ł���B���쐫�S�[�ד���̃z���^�[�S�d�}�ɂ��ώ@������A�P�̐S�[�����O���k���_�@�Ƃ��ĐS�[�ד����U������錻�ۂ��ώ@����Ă���B���̂悤�ȐS�[�ד��o���̈������ƂȂ�ُ��������́A�x�Ö��ǂ��琶����ꍇ���������Ƃ����炩�ɂȂ����BHaissaguerre��i�P�X�X�W�j�́A�S�[�ד��̎��R���삪�p�������ŁA���̈������ƂȂ����ُ��������̋N����mapping�@��p���Č������A���\�Ɏ����悤�Ȑ��т������A���쐫�S�[�ד��̋N���Ƃ��Ĕx�Ö����ُ̈������̏d�v�����w�E�����B
| ���쐫�S�[�ד��J�n�̋N���ƂȂ����ُ������̕��� | ||||
| ���� | �ᐔ | �� | ||
| �S�[���R�� | �E�[ | �R | �S�D�R | �T�D�V |
| ���[��� | �P | �P�D�S | ||
| �x�� | ����x�� | �R�P | �S�S�D�X | �X�S�D�R |
| �E��x�� | �P�V | �Q�S�D�U | ||
| �����x�� | �P | �P�T�D�X | ||
| �E���x�� | �U | �W�D�V | ||
| �v | �U�X | �P�O�O�D�O | ||
�@�iHaissaguerre,M. et a..: New Eng.J. Med. 339:659,1998)
�@�����A�S�[�ד��ێ��@�\�Ƃ��ẮA�����̕s�K���ȃ��G���g���[�@�imultiple reentry)�@�������ł���Ƃ���l�������S�ɂȂ��Ă���B���}�́A�S�[�ד��� multiple reentry ����͌^�I�Ɏ��������̂ł���B
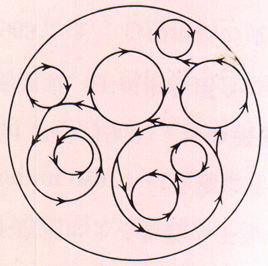
�@�g���K�[�@���i���Nj@���j�ɂ�萶�����S�[�����́A�S�[�̕s�����ɂ�薳���̊��̂��߂ɑ����̏ꏊ�ŋ����g�̃��G���g���[���N����Adau����ter�@wave�idaughter�����j�͋}���ɂ��̐������X�Ƀ��G���g���[�𑱂��A�������Đ����������̃��G���g���[�ɂ��S�[���s�K���Ɏ��k���A�S�[�ד����o���A�ێ������B
�@���}�́C����ɂ��S�[�ד��̑����������B�S�[�ד�������Ƌ��ɋ}���ɑ��������Ԃ��悭������Ă���B
 |
|
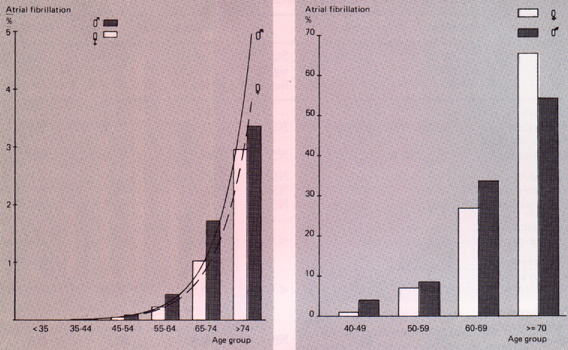
| �N��E���ʕ��ފe�Q�ɂ����� �S�[�ד��̕p�x �i���F�j���C���F�����j |
�S�[�ד���̔N��E ���ʕp�x �@�i���F�j���A���F�����j |
�iKulbertus HE��FAtrial fibrillation in eldery patients. Ed. Kulbertus HE��FAtrial fibrillation, AB Hassle, Molndal,1982)
�S�D�S�[�ד��̕���
�@�P�j�o�߂ɂ�镪��
�@�@�@�i�P�j���쐫�S�[�ד��F�S�[�ד�������ԂɁA�S�[�̓d�C�I�����f�����O���N����A�Q���A������������Ȃ�A���ɂ͖����S�[�ד��Ɉڍs����B
�@�@�@�i�Q�j�����S�[�ד��F�����I�ɐS�[�ד��������B
�@�Q�j�S�����ɂ�镪�ށ@
�@�@�@�i�P�j�p�����S�[�ד��F�S��������і����������������A�S�����i�A�ċz�����i����B�����̏Ǐ�͐g�̘J��ɂ�葝������B
�@�@�@�i�Q�j�������S�[�ד��F�S�����̏��Ȃ��S�[�ד��ŁA���s�S�nj�Q�̈�\���ł���ꍇ������B�S�[�ɍL�͂ȕa�ς�����悤�ȏꍇ�ɔF�߂���B
�T�D�S�[�ד��̐S�d�}�̎���
�@�ȉ��Ɋe��̐S�[�ד���̐S�d�}�������B�S�[�ד��̐S�d�}�̓����̂P�͐�ΐ��s�����ŁA�S���K������F�߂Ȃ��s�������������ߖ��f�݂̂���ł������̏ꍇ�ɐf�f�\�ł���B�������S�[�ד��Ɋ��S�[���u���b�N����������ƁA�S���͊ɏ��Ȑ����ƂȂ�s�����͔F�߂��Ȃ��Ȃ�B
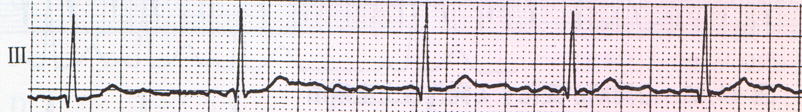
�@�P�j�@�ʏ�̐S�[�ד�
�@�S�d�}����
�@��r�I�ɐS���������Ȃ��S�[�ד��ł���B�o�g�̑O�Ɉ��Ԋu�Ő�s����o�g��F�߂��A����̕s�K���ȓ��h��F�߂�i�S�[�ד��g�A���g�j�B�S���Q�̏o���͕s�K���Ő�ΐ��s�����iarrhythmia
absoluta)�@�������B�r�s�|�s���ɂ͕ω����Ȃ��B
�@�Q�j�p�����S�[�ד�
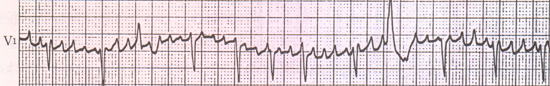
�@�S�d�}�����F
�@���g�̐U���������B���g�͒ʏ�u�P�C�Q�ŐU���������B�ꌩ�A���g���傫�����߂ɐS�[�e���̂e�g�ɗގ����邪�A�ڂ�������ƐS�[�g�̌`�͕s�����ł��邽�߁A�e�g�ł͂Ȃ��A���g�ł���ƍl������B��R�C�X�S���̕ό`�����S���Q�͕ύs���S�����`���ɂ��S���Q�̕ό`�ł���B��ʂɕύs���S�����`���ɂ��S���Q�̕ό`�͉E�r�u���b�N�^�������B
�@�R�j�@�������S�[�ד�

�@�S�d�}�����F
�@���������邽�߂ɁA�ꌩ�A�����Ɍ����邪�A�ڂ����ώ@����Ɛ�ΐ��s����������A�������S�[�ד��Ɛf�f�����B
�@�S�j�@���쐫�S�[�ד� �iparoxysmal atrial fibrillation, PAF)
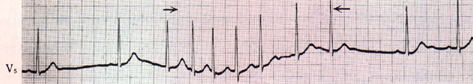
�@�S�d�}�����F
�@���Ŏ������͈͂����쐫�S�[�ד��ł���B�S�[�ד�����͐S�[�����O���k�Ŏn�܂�A�x�~���̌�ɓ����Y���Ɉڍs���Ă���B�{��̂悤�Ɏ������ɂ߂ĒZ�����쐫�S�[�ד�����ߐ��S�[�ד��itransient
atrial�@fibillation)�@�ƌĂԏꍇ������B
�@�T�j�@���S�[���u���b�N���S�[�ד�
![]()
�@�@�S�d�}�����F
�@�o�g�͂Ȃ����g��F�߂邪�A�S���͊ɏ��ŋK���I�ł���B�S�����k�́A�[���ڍ��������̎����\�ňێ�����Ă���B
�@�S�[�ד��̎��ẤA
�@�@�@�i�P�j���쐫�S�[�ד��̎��ÁA
�@�@�@�i�Q�j�����S�[�ד��̎��ÁA
�@�̂Q�ɕ����čl����K�v������B�܂��S�[�ד��̎��Â̍ۂɂ́A�d�v�ȍ����ǂƂ��Ă̓����ǐ��i�]�ǐ��A�]�[�ǁj��\�h���邱�Ƃ��K�v�ł���B
�@
�@�@�P�j���쐫�S�[�ד��̎���
�@�@�@���쐫�S�[�ד��͕p�����S�[�ד��̌`���Ƃ�A�����������������A���҂͐S�����i�A�J�쎞�ċz����Ȃǂ̎��o�Ǐ�������i����Ⴊ�������߁A
�@�@�@�i�P�j�������A�܂���
�@ �@ �i�Q�j��������,��}��K�v������B
�@
�@�S�[�ד����삪���쐫�ł��邩�ǂ����͎��Ԍo�߂����Ȃ��ƕ�����Ȃ��B���̂��߁A���쐫�S�[�ד��Ƃ������t�����u�}���S�[�ד��@(acute
atrial fibrillation) �Ƃ����\�����Ó��ł���Ƃ̍l��������B�]���͔��쐫�ɏo�����A�Ăѓ����������Ă������̂��A����̔�����_�@�ɖ����S�[�ד��Ɉڍs����\�����[������B
�@���쐫�S�[�ד������������ƐS�[�̓d�C�I�����f�����O���N����A���ꂪ�������̌����ƂȂ邱�Ƃ��w�E����Ă��邽�߁A�ד�����o����A�o���邾�������Ɏ��Â��n�߂�K�v������B�@
�@���쐫�S�[�ד��̎��Âɂ��ẮA2001�N�ɔ��\���ꂽ�č��S���a�w��iACC)�A�č��S������(AHA)����щ��B�S���a�w��(ESC)�ɂ��K�C�h���C�����������₷���B�@���̃K�C�h���C���ł͐V�K���ǐS�[�ד��쐫�i��ߐ��j�S�[�ד��Ǝ������S�[�ד��ɕ��ނ��A���̎��Õ��j�����}�̔@�������Ă���B
| �S�[�ד��̔��ǃp�^�[���iACC/]AGHA/ESC�K�C�h���C���j |
�@ ���쐫�i��ߐ��j�S�[�ד��Ƃ�24���Ԉȓ��i�����Ƃ��P�T�ȓ��j�Ɏ��R��~����S�[�ד��ŁA���̂悤�Ȕ���͒ጌ���A�S�s�S�A���S�ǂȂǂ̏d�ĂȏǏȂ���Ύ��Â̕K�v���Ȃ��A����������͍R�s������ɂ��ێ����Â�K�v�Ƃ��Ȃ��B�������S�[�ד��Ƃ͎��R���������X���������Ȃ���������S�[�ד��ł���B
�@�������Ȃ���}���S�[�ד�����ŗ��@�����ꍇ�A���ꂪ��ߐ��ł��邩�������ł��邩�͕�����Ȃ����߁A���ׂĂ̋}���S�[�ד��͎������S�[�ד��Ƃ��đΉ�����B���Ȃ킿�A����҂⍇�������Ȃǂ�����A�����S�[�ד��Ɉڍs���Ă��ǂ��Ǝv�����ł͐S�����̃R���g���[��(rate
control)�ƍR�Ì���Ö@���s���B
�@����ȊO�̔��ǂS�W���Ԉȓ��̐S�[�ד���ł́A�S�[�������̑��݂���\�����Ⴂ���߁A�R�s������ɂ�铴��������}��B���̍ہA���������ɐ��������ꍇ�ɂ́A�����Ԃ̍R�s������ɂ�鎡�Â͕s�v�ł���B
�@���쐫�S�[�ד��̓��������̂��߂ɂ́A�R�s������Ò��Ö@�ƃs���W�J�C�j�h�A�s�����m�[���̂悤�ȏ����ǂ���̋z�������悭�A���̓����p���������T�Q�R�s������̒P��o�����^�@���s����B
�@�i�P�j�R�s������Ò��Ö@
�@���쐫�S�[�ד��̓��������ɗp���鏔��̐Ò��p�R�s������̎�ނƎg�p�@����ѓ����������������\�Ɏ����B�@
| �R�s������ | ���i�� | �܌^ | ���^�@ |
| �v���J�C���A�~�h | �A�~�T���� | �P��10%(100mg/ml)1,2ml | 50-100mg/���̑��x��1000mg�Ò� |
| �W�\�s���~�h | ���X���_���o | 1��50mg,5ml | 1.5-2mg/kg���ɏ��ɐÒ� |
| �V�x���]���� | �V�x�m�[�� | 1��70mg,5ml | 1.5mg/kg���ɏ��ɐÒ� |
| �s���W�J�C�j�h | �T�����Y�� | 1��50mg,�@5ml | 0.75mg/kg��10���ŐÒ� |
| �A�v�����W�� | �A�X�y�m�� | 1��50mg,5ml; 100mg,10ml |
�@5%���t��10�{���,1.5-2.0ml/kg���@�@�@�@ 5-10ml/���Ŋɏ��ɐÒ� |
| �t���J�C�j�h | �^���{�R�[�� | �P��50mg,5ml | 2mg/kg�10�i�`30�j���ŐÒ� |
����̍R�s������Ò��ɂ�锭�쐫�S�[�ד��̓���������
| / | �R�s������ | �����������i���j |
| ���Ăł̐��� �i�Ò�1-2���Ԉȓ��̒�~�j |
�v���J�C���A�~�h | �Q�O�|�V�P |
| �W�\�s���~�h | �Q�W�|�U�W | |
| �A�v�����W�� | �Q�Q�|�S�P | |
| �V�x���]���� | �T�P�|�V�W | |
| �t���J�C�j�h | �T�V�|�X�Q | |
| �s���W�J�C�j�h | �R�X�|�T�T | |
| �����E���� �i�Ò�30���ȓ��̒�~�j |
�W�\�s���~�h | �Q�X |
| �A�v�����W�� | �Q�Q | |
| �V�x���]���� | �T�Q | |
| ���̑��̉䂪���ł̕� | �t���J�C�j�h | �S�U |
| �s���W�J�C�j�h | �R�W |
�i�������A�������F�S�[�ד��̖��ÁA�����̎��Á@�P�O�i�V�j�F�V�Q�T�|�V�R�Q�C�Q�O�O�Q�j
�@�i�Q�j�R�s������P��o�����^�@
���쐫�S�[�ד��̒P��o�����^�ɂ�铴�������ɂ̓s���W�J�C�j�h�i�T�����Y���A�P��25,50m���j�A�s�����m�[���i�s���m�[���A�P�J�v�Z��50,100mg�j�A�t���J�C�j�h�i�^���{�R�[���A�P��50,100mg�j�Ȃǂ��p������B�s���W�J�C�j�h100mg
�̒P��o�����^�łR���Ԉȓ��̓���������������73%�ƕ���Ă���i���w�F�S���[�V���O8::240,1992)
�B
�@�i�R�j�R�Ì���Ö@
�@�S�[�ד��o����S�W���Ԉȏ�o�߂�����ł́A���S�[�i���Ƃɍ��S���j���Ɍ������`������Ă���\��������B���̂悤�ȗ�ł́A�������������ۂɐS�����������������ē����ǐ��i���Ƃɔ]�ǐ��j���N�����댯���������߁A�o�H���S�G�R�[�@��p���ĐS�[�������̗L���ɂ��Č�������B���S�[��������F�߂��ꍇ�ɂ�warfarin�ɂ��R�ÌŗÖ@���s���A�v���g�����r�����Ԃ𑪒肵��INR�l(international
normalized ratio)���@2.0�|3.0�@(70�Έȏ�̍��N�҂ł�1.5�|2.5)�̊Ԃɕۂ悤�ɋÌ��\�߂���@(warfarin�g�p�@�ɂ��Ă͌�q�j�B
�Q�j �Ĕ����J��Ԃ��S�[�ד��̎���
�@���̂悤�ȗ�ł͓��������ɐ������Ă��Ĕ��̉\�����������߁AACC/AHA/ESC �K�C�h���C���ł͐S�[�ד����쎞�̎��o�Ǐ�̗L���E���x�ɂ�艺�}�Ɏ����悤�Ȏw�j�������Ă���B���Ǐ��ł͐S�����R���g���[���ƍR�Ì���Ö@���s���A�R�s������͓��^���Ȃ��B�Ǐd���ꍇ�ɂ� �S�����R���g���[���ƍR�Ì���Ö@���s���A�R�s������ɂ�铴���������s���B
| �Ĕ����J��Ԃ��S�[�ד��̖Ö@�iACC/AHA/ESC�K�C�h���C��,2001) |
�@�R�j������/�������S�[�ד��̍R�s�����Ö@
�@�������^�������S�[�ד��̓��������̂��߂̍R�s�����Ö@�Ƃ��āAACC/AHA/ESC�K�C�h���C���͉��}�Ɏ����悤�Ȗ�ܑI���w�j�������Ă���B���{�z��w��R�s������K�C�h���C���ψ���������Ă���S�[�ד��̓��������̂��߂̍R�s������I�����ACC/AHA/ESC�K�C�h���C���Ƃ͂��Ȃ�قȂ�B
| ������/�������S�[�ד��̖w�I���ד��̍ۂ̍R�s������̑I����iACC/AHS/ESC�K�C�h���C���j |
�@�@���{�z��w��R�s������K�C�h���C���ψ���́A�S����99/���ȉ��̔��쐫�S�[�ד��̖w�I���ד��@�Ƃ��ĉ��L�̂悤�ȕ��@�����߂Ă���B���Ȃ킿�A�A���R�[�����A�S����p�㐫�A�b��B�@�\���i�NjN���̔��쐫�S�[�ד��ɂ͂܂����Ւf���p����B���Ւf���Ⴀ�邢�͂����̌����ɂ��Ȃ����쐫�S�[�ד���ł́A�܂��S�@�\��]�����C���̒��x�ɂ�艺�\�Ɏ����悤�ȍR�s������I�����邱�Ƃ��������Ă���B�S������100/���ȏ�̗�ɂ��ẮA�V���b�N�Ǐ�̗L���ɒ��ӂ��A�V���b�N�ǏL��Β������ד����s���i�w�p�����O���^�j�A�V���b�N�ǏȂ��ꍇ�͖�܂ɂ��S�����R���g���[�����s���B���̍ہA�v�o�v�nj�Q�łȂ��ꍇ�́A�S�@�\�����ł̓��Ւf��܂��̓W�S�L����p���A�S�s�S�������ł̓W�S�L�V����p����B
���{�z��w��R�s������K�C�h���C���ψ���ɂ�锭�쐫�S�[�ד��̖w�I���ד����̍R�s������̑I����i�S����<99/���j
| �S�@�\ | ���I�� | ���I�� |
| ���� | slow drug | intermediate drug |
| �W�\�s���~�h�A�V�x���]�����A�s���W�J�C�j�h �i�t���J�C�j�h�A�s�����m�[���j |
�v���J�C���A�~�h�A�L�j�W���A �v���p�t�F�m���A�A�v�����W�� |
|
| �y�x�ቺ | intermediatge drug | slow drug |
| �v���J�C���A�~�h�A�L�j�W���A�v���p�t�F�m���A �A�v�����W�� |
�W�\�s���~�h�A�V�x���]�����A�s���W�J�C�j�h�A �i�t���J�C�j�h�A�s�����m�[���j |
|
| �����x�ȏ� �ቺ |
intermediate drugs (���Ւf��p������̂������j | |
| �v���J�C���A�~�h�A�L�j�W���A�A�v�����W�� | ||
�@�@�@�i �@�@�j���́A���N�ی����K�p�B
�@�@�@slow, intermediatge, fast : Na�{�`���l���Ƃ̌����E�𗣑��x���x�����́A���ԓI�Ȃ��́A�������́B
�@�@�i���쑏�F�R�s������K�C�h���C���A���C�t���f�B�R���A�����A�Q�O�O�O�j
�S�j�ד�����o�����ԑтɂ��R�s������̑I��
�@�@�S�[�ד�����̔���o�����ԑт͊e�l�ɂ�����������A���L�̂悤�ɂR�^�ɕ�������B
�@�@�i�P�j��^�i�����_�o�^�j�F���삪�ߌ�V������ߑO�V���܂ł̊Ԃɔ��ǂ���^�ŁA�����_�o�ْ������̔��ǂɊ֗^���Ă���Ǝv���A�W�\�s���~�h�������~�A�������ێ��ɗD��Ă���B
�@�@�i�Q�j���^�i�����_�o�^�j�F���삪�ߑO�V������ߌ�V���܂ł̊Ԃɔ��ǂ���^�ŁA�����_�o�ْ������̔��ǂɊ֗^����ƍl������B�A�v�����W���A�v���J�C���A�~�h�B�x�v���W���Ȃǂ̗L�����������B
�@�@�i�R�j�����^�F���Ɏ��ԓI���ِ����Ȃ����̂ŃV�x���]�����̗L�����������B
�@�T�j�S�����R���g���[��
�@ACC/AHA/ESC�K�C�h���C���ł́A�}�����̐S�����R���g���[���̂��߂ɂ�Ca�h�R��܂��̓��Ւf��Ò��A�����S�[�ד��̐S�����R���g���[���ɂ͂����̖�܂̓����܂��ͼ��ؽ���Ca�h�R��i�܂��̓��Ւf��j�̕��p�����߂Ă���B�S�����R���g���[���̖ڕW�l�Ƃ��Ă͈��Î�60�`90/���A�y�x�`�����x�J�쎞��110�`120/���A�z���^�[�S�d�}�̕��ϐS����50�`90�@(��85�j/���A�P�����S�����P�R���ȉ����]�܂����B
�@�U�j�v�o�v�nj�Q�ɍ��������S�[
�@Kent���Ȃǂ̕��`���H�͈�ʐS�ł��邽�߁A�[�����߂ɔ�ׂĕs�������Z�����A�S�[�ד��̍ۂɂ͒������p�����A�S������300/���ȏ�ɒB����������B���̌��ʁA�S�����ɕs�K���ȕs����������ĐS���ד���U�����A�}�����������Ȃ��Ȃ��B���̂悤�ȗ�̐S�[�ד�����̍ۂɂ̓W�\�s���~�h�C�W�M�^���X�܂̎g�p�͋֊��ŁA���`���H�̕s��������������悤�ȍR�s������i�v���J�C���A�~�h�A�t���J�C�j�h�A�A�v�����W���Ȃǁj�̐Ò����s�����A�܂��͒����V���b�N�Ö@���s���B�S�[�ד����쎞�̍ŒZRR�Ԋu����250msce�̏ꍇ�͊댯�ȏ�Ԃł���A�����V���b�N�Ö@�����߂���B���̂悤�ȗ�ł͔���Ԍ����ɕ��`���H��ablation���s���Ă������Ƃ��K�v�ł���B
�V�j ���쐫�S�[�ד��̖����S�[�ד��ւ̈ڍs���ƈڍs����
�@�@�@�T�D���쐫�S�[�ד��̖����S�[�ד��ւ̈ڍs��
| ��b���� | ���쐫�S�[�ד� ���@�����S�[�ד� |
| �������S���� | �Q�V�� |
| ���������S���� | �S�O�� |
| �����������������S���� | �T�� |
| ���E�}�`���S���� | �U�U�� |
| �b��B�@�\���i�� | �R�Q�� |
| �}���S�؍[�Ǐ� | �Q�T�� |
�@�U�D���쐫�S�[�ד��̏������疝���S�[�ד��ւ̈ڍs����
| ��b���� | �ڍs���� |
| ���������S���� | �R�R�`�U�P�J�� |
| �������S���� | �P�Q�`�R�Q�J�� |
| ���E�}�`���S���� | |
| ���� | �R�S�J�� |
�@�W�j�@�����S�[�ד��̎���
�@�����S�[�ד��̎��Â̊�{�́A�]���͉��L�̂Q���ڂɒu����Ă����B
�@�@�@�@�i�P�j�@�S�����̃R���g���[���A
�@�@�@�@�i�Q�j�@�����ǐ��ǁi�]�ǐ��A�]�[�ǁj�̗\�h�A
�@���݂ł�����炪���Ö@�̎嗬���Ȃ����A�ߔN�A�����S�[�ד����I�ɓ�������������@�����Ȃ�̐��ʂ����߂�悤�ɂȂ����B�@�@�@
�@�T�D�S�����̃R���g���[��
�@�@�@���̖ړI�ɂ́B���Ւf��A�b���h�R������������B���`���W�S�L�V���i���j���s�h�A�P��0.1mg,�@0.05mg)���ϖ��ǍD�Ȃ��߂悭�p������B�}���Ȃ��ꍇ�́A�P���P�����̌p�����^�ł悢���A�Ǐ����}���ꍇ�͍ŏ��̂R���Ԃ͂R���i�P����0.3mg�A���R�j�A�Ȍ�͂P���P����p����B�@
�@�U�D�����S�[�ד��ɂ�����]�ǐ��̗\�h
�@�@�@�����S�[�ד��́A�]�[�ǁi�]�ǐ��j�̏d�v�Ȋ댯���q�ł���A�����S�[�ד��ɍ��������]�[�ǂ́A�]�������̓����d�����ǂȂ��������ɂ��]�[�ǂɔ�ׂč[�Ǒ����傫���\����d�Ăł���B��ʓI�ɁA�����S�[�ד��ɋN������]�ǐ��ɂ͉��L�̂悤�ȓ���������B
�@�@�@�@�i�P�j�@�U�O�Έȏ�̔N��w�ɂ�����]���Ǐ�Q���ɐ�߂�]�[�ǂ̕p�x�͂V�T���ł���B
�@�@�@�@�i�Q�j�@�]�[�ǒ��ɐ�߂�]�ǐ��̕p�x�͂P�T�`�Q�O���ł���B
�@�@�@�@�i�R�j�@�]�ǐ��̊�b�����Ƃ��Ă͔�ٖ��ǐ��S�[�ד����ł������i�S�T���A5%/�N�j�B
�@�@�@�@�i�S�j�@�S�[�ד���ɂ����铮���ǐ��̕��ʂƂ��Ă͔]�i�R�R�`�W�Q���j�A�l���i�P�R�`�R�R���j�A�����i�S�`�S�Q���j�������B
�@�@�@�@�i�T�j�@�g�p��܂ɂ��ẮA���[�t�A�������ł��L���ŁA�A�X�s�����̌��ʂ̓��[�t�A�����ɗ��B�����ǐ��̏o�����̓��[�t�A�����ł͂P�D�T���ł��邪�A�A�X�s�����ł͂U�D�R�����x�ł���B
�@�V�D�O�����[�t�A�����Ö@
�@�@�@�����S�[�ד���͎��o�Ǐ��Ȃ��O���f�Â��啪�����߂�B���������ă��[�t�A�����Ö@����Ƃ��ĊO���ōs���B���̍ۂ͏��ʓ��^����͂��߁A�Ì��\���ώ@���Ȃ��班�ʂ����ʂ��Ăh�m�q�l(international
normalized ratio)��2.0�|3.0�ɕۂB���Ҍ����̃v���g�����r�����ԁi�o�s�j�𐳏파���̂���ŏ����ăv���g�����r�����Ԕ�(prothrombin
time ratio,�@PTR) �����߁A����ɓY�t����Ă��銷�Z�\�łh�m�q�����߂�B�h�m�q�̐���l�͂P�D�O�ŁA�o�s����������ɂ�Ăh�m�q�͑傫���Ȃ�B���\�ɂh�m�q�l�g�g�����{�e�X�g�l�i���j�Ƃ̊W�������B
�h�m�q�l�ƃg�����{�e�X�g�l�i�s�s�j�Ƃ̊W
| �h�m�q | �g�����{�e�X�g�i�s�s�j�i���j |
| �P�D�O | �W�P�D�O |
| �P�D�T | �Q�V�D�Q |
| �Q�D�O | �P�U�D�R |
| �Q�D�T | �P�P�D�W |
| �R�D�O | �X�D�Q |
| �R�D�T | �V�D�V |
| �S�D�O | �U�D�T |
| �S�D�T | �T�D�V |
| �T�D�O | �S�D�X |
INR:�@international normalized ratio, TT:
thrombo test
(�萳�F�A�דc����F�O�쐳��ďC�A���[�t�@�����A���f�B�J���W���[�i���ЁA�����A�P�X�X�O�j
�@�k���l�O�����[�t�A�����Ö@�̎��{�@�@
�@�@�P�j��P�@
�@�@�@(1)�@���[�t�@�����@1mg/�����Q�T�ԏ�������B
�@�@�@(2)�@�v���g�����r�����ԁi�h�m�q�l�j������Q�T�ɂP�x���{���Ȃ���A�h�m�q�@2.0�|3.0��ڕW�Ƃ��ē��^�ʂ��Q�T����0.25�`0.5mg/������������B
�@�@�@(3)�@���肵����v���g�����r�����ԁi�h�m�q�j������Q�J���Ɉ�x���{����B
�@�@�Q�j��Q�@�@�F
�@�@�@(1)�@�v���g�����r�����Ԃ𑪒肵�Ăh�m�q�����߁A���ꂪ�P�D�O�O��ł�����[�t�A�����i�P���P�����j������3mg/����^����i�P���P��A���H��j�B
�@�@�@(2)�@��Q���Ȍ��1mg/����^���A�����v���g�����r�����Ԃ𑪒肵�C�h�m�q���Q�D�O�|�R�D�O�̊Ԃ̒l���ێ��ł���悤�ɓ��^�ʂ߂���B
�@�@�@(3)�@���^�ʂ̑�����0.5mg/���B
�@�@�@(4)�@�P�T�ň����ɓ���B���̌�̓g�����{�e�X�g���{�Ԋu���P�T���Q�T���P�����Q���Ɖ�������B�@
�X�j�S�[�ד��̔�Ö@
�@�@�S�[�ד��̔�Ö@�Ƃ��Ă͎��̂悤�ȕ��@������B
�@�@(1)�@maze��p:�@Cox��(1991)�ɂ��n�߂�ꂽ���@�ŁA�S�[����H��ɐؒf���ĐS�[�ד��̌����ƂȂ��Ă��郊�G���g���[��H���Ւf�����p�ł���imaze�����H�j�B
�@�@(2)�@catheter maze �@�F�J�e�[�e���Ďܖ@�ɂ�藼�S�[�ɐ����ablation���s���Amaze��p�ɗގ�������Ԃ�S�[�ɍ쐬����B
�@�@(3) �x�Ö�ablation,�@�x�Ö��u���@�F�x�Ö����̉ߕq�Ȉُ�������catheter�@ablation�@��p���ċǏ��I�ɏĎ܂�����@�ł���B���̕��@�ł́A�x�Ö�����Ȃǂ̍����ǂ��N�����₷�����߁A�x�Ö��ƍ��S�[�Ƃ̓d�C�I�A���H���Ւf������@���l�Ă���A��r�I�����������������Ă���i�x�Ö��u���@�j�B
�@�F�J�́A�x�Ö��u��ablation�̐������쐫�S�[�ד�47��Ō������A���ςW����̌o�ߊώ@���Ԓ��̖������ł̐������͂U�W���A�R�s�����^���ł̐�������81%�ł��������Ƃ���Ă���i�F�J�_��Y�F�S�[�ד��̃J�e�[�e���A�u���[�V�����A�����̎���,
10 (7): 733�`738 , 2002) �B
�@�S�[�ד��ł́A�S�[�̂܂Ƃ܂������k���Ȃ����߁A�������ɔ�ׂČ��s���ԓI�ɕs���ł���A�g�̘J��Ȃǂ̍ۂɕp���ɂȂ�Ղ��A������������������ƐS���̋@�B�I��������������Q�����B�܂��S�[�ד��ł͐S�[���������S�����]�ǐ��i�������]�[�ǁj�̌����ƂȂ�B���̂��߂ɐS�[�ד��ł͓���������}���邱�Ƃ��������A�R�s������ɂ�torsade
de pointes�Ȃǂ̏d�Ăȕs�����U����p������A���S����ꍇ�������ď��Ȃ��Ȃ��B�܂��A�R�s������Ȃǂ�p���ĐS�[�ד��̓��������ɐ������Ă��A�Ĕ����������������B
�@���\�́A���������ɐ���������A�e��̍R�s������̌p���������s������ɂ�����P�N����тQ�N�̊ώ@���Ԃɂ����铴�����ێ����i���j�������B�P�N��ɂ����铴�����ێ�����35�`51%,
�Q�N��̂����21�`47%�ō����ɍĔ����Ă���B
�R�s������̓������ێ�����
| �R�s������ | �������ێ����i���j | |
| �P�N�� | �Q�N�� | |
| �W�\�s���~�h | �T�P | �S�V |
| �A�v�����W�� | �R�T | �Q�P |
| �V�x���]���� | �S�V | �R�V |
�i�������A�������F�S�[�ד��̖��ÁA�����̎��Á@�P�O�i�V�j�F�V�Q�T�|�V�R�Q�C�Q�O�O�Q�j
�@���̂��߁A�S�[�ד���̊Ǘ��ɓ���������}���������悢�̂��A���邢�͐S�����Y���͐S�[�ד��̂܂܂Ƃ��A�S�����R���g���[���ƍR�Ì��^�ɂ�錌���E�ǐ��ǂ̗\�h��}���������悢�̂��͓�����ŁAevidence�Ɋ�Â����M�����������������]�܂�Ă����B
���̖��Ɋւ����K�͗Տ��������т��ŋߔ��\���ꂽ�B���̌�����AFFIRM�@Study�iAtrial
Fibrillation Follow-up Investigation of Rhythm
Managemet)�Ɩ��t�����A�S�[�ד���ɂ����ă��Y���R���g���[���i�������ێ��j�ƃ��[�g�R���g���[���i�S�����R���g���[���j�̉��ꂪ�悢����4,060��̐S�[�ד���ɂ��Č����������{���������ł���B
�@���̌����́A�]�����̊댯���q��L����65�Έȏ�̐S�[�ד�������Y���R���g���[���Q(2,033��j�ƃ��[�g�R���g���[���Q(2,027��j�ɕ����A�ꎟ�G���h�|�C���g���S�A�G���h�|�C���g�����S�A���ǂ��c���]���Ǐ�Q�i�܂��͋������]�ǁj�A�d�Ăȏo���A�S��~�ɒu���ė��Q�Ԃ̔�r���s�����B
�@���̌��ʁA�ꎟ�G���h�|�C���g�ɂ��ẮA���[�g�R���g���[���Q�̕����A���Y���R���g���[���Q���������S�������Ⴂ�X����F�߂����̂́A���Q�ԂɗL�Ӎ��͔F�߂Ȃ������B�G���h�|�C���g�ɂ��Ă����l�ɗ��Q�ԂɗL�Ӎ���F�߂Ă��Ȃ��B
�@�܂����Q�ɂ���QO L (quolity of life)�����Ă��邪�A�S�o�߂̊e���_�ɂ����ė��Q�͗ގ��������т��������B����ɐ����A�������ێ��A���ד�����{�A����t����ꂽ�R�s������̕��p�ێ����ꎟ�G���h�|�C���g�Ƃ��Ċe�R�s������̃T�u��͂��s���A�A�~�I�_�������ł����ʓI�ł������Ƃ̌��ʂ��B
�@AFFIRM�����ɂ��ẮA�Ώۂ̒�ߕ��A�g�p�����R�s������̎�ނȂǂɎ�̖�肪����Ƃ̎w�E�����邪�A�v���I�s�����U���̊댯��N���čR�s������ɂ�鏜�ד���}������A�S�������߂ƍR�Ì���Ö@�Ōo�߂��ώ@����̂ŏ\���ȏꍇ�����邱�Ƃ������Ă���A���ɏd�v�ȈӋ`��L���錤���ł���B
�@�@